医疗器械发布规则解读
更新时间:2021年10月25日
1 概述
医疗器械是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括所需要的计算机软件。用户提交相应的证件后可在中国制造网上发布此类产品。
2 禁止发布产品列举
2.1食品药品监督管理部门依法明令禁止生产、销售和使用的医疗器械产品;
2.2医疗机构研制的在医疗机构内部使用的医疗器械。
3 允许发布产品
3.1 入驻要求:
3.1.1
三类医疗器械
| 工厂 | 贸易公司 |
| 营业执照 | 营业执照 |
| 《医疗器械生产企业许可证》或者《医疗器械产品出口销售证明书》 | 《 医疗器械经营企业许可证》或者供货工厂的《医疗器械生产企业许可证》或者《医疗器械产品出口销售证明书》 |
| 《医疗器械注册证》或者国外认证证书 | 《医疗器械注册证》或者国外认证证书 |
| 供货证明 |
3.1.2二类医疗器械:
| 工厂 | 贸易公司 |
| 营业执照 | 营业执照 |
| 《医疗器械生产企业许可证》或者《医疗器械产品出口销售证明书》 | 《第二类医疗器械经营备案凭证》或者供货工厂的《医疗器械生产企业许可证》或者《医疗器械产品出口销售证明书》 |
| 《医疗器械注册证》或者国外认证证书 | 《医疗器械注册证》或者国外认证证书 |
| 供货证明 |
3.1.3一类医疗器械
| 工厂 | 贸易公司 |
| 营业执照 | 营业执照 |
| 《第一类医疗器械生产备案凭证》或者国外认证证书 | 供货工厂的《第一类医疗器械生产备案凭证》或者国外认证证书 |
| 供货证明 |
3.2 证件示例




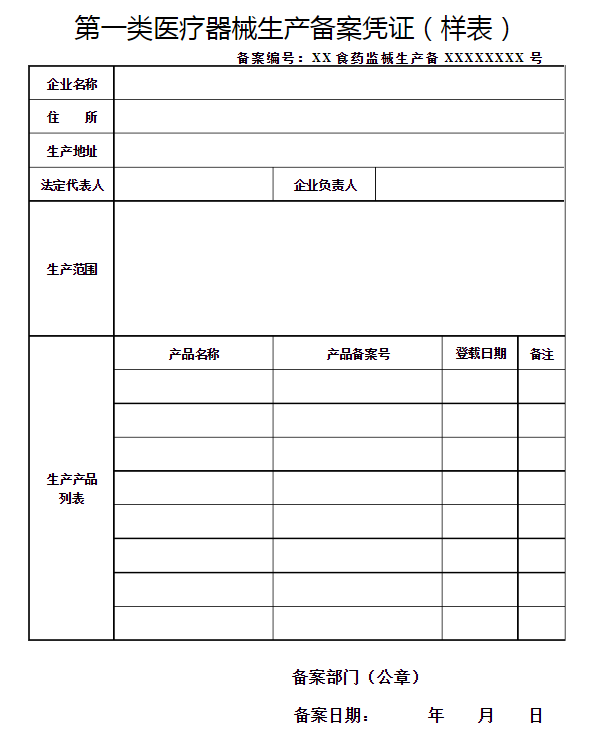
3.3 发布要求
3.3.1医疗器械产品注册证明文件中有禁忌内容、注意事项的,应在信息中标明“禁忌内容或注意事项详见说明书”。
3.3.2医疗器械信息中有关产品名称、适用范围、性能结构及组成、作用机理等内容应当以食品药品监督管理部门批准的产品注册证明文件为准。
3.3.3推荐给个人使用的医疗器械产品信息,必须标明“Please read the instruction carefully and follow it, or please purchase and use those drugs under the guidance of the medical staff(请仔细阅读产品说明书或在医务人员的指导下购买和使用)”。
3.3.4医疗器械信息中涉及改善和增强性功能内容的,必须与经批准的医疗器械注册证明文件中的适用范围完全一致,不得出现表现性器官的内容。
3.3.5医疗器械信息中不得含有利用医药科研单位、学术机构、医疗机构或者专家、医生、患者的名义和形象作证明的内容。
3.3.6医疗器械信息中不得含有军队单位或者军队人员的名义、形象。
3.3.7医疗器械信息不得以儿童为诉求对象,不得以儿童的名义介绍医疗器械,如“爸爸帮我买了XX,再也不用担心得近视眼啦”等。
3.3.8医疗器械信息中有关适用范围和功效等内容的宣传应当科学准确,不得出现下列情形:
3.3.8.1含有表示功效的断言或者保证的,如“绝对有效”等;
3.3.8.2说明有效率和治愈率的,如“治愈率达100%”等;
3.3.8.3与其他医疗器械产品、药品或其他治疗方法的功效和安全性对比;
3.3.8.4在向个人推荐使用的医疗器械信息中,利用消费者缺乏医疗器械专业、技术知识和经验的弱点,使用超出产品注册证明文件以外的专业化术语或不科学的用语描述该产品的特征或作用机理;
3.3.8.5含有无法证实其科学性的所谓“研究发现”、“实验或数据证明”等方面的内容;
违反科学规律,明示或暗示包治百病、适应所有症状的;
3.3.8.6含有“安全”、“无毒副作用”、“无效退款”、“无依赖”、“保险公司承保”等承诺性用语;
3.3.8.7含有“唯一”、“精确”、“最新技术”、“最先进科学”、“国家级产品”、“填补国内空白”等绝对化或排他性的用语;
3.3.8.8声称或暗示该医疗器械为正常生活或治疗病症所必须等内容的,如“家庭必备”“颈椎病必备”等;
3.3.8.9含有明示或暗示该医疗器械能应付现代紧张生活或升学、考试的需要,能帮助改善或提高成绩,能使精力旺盛、增强竞争力、能增高、能益智等内容,如“使用三周,赶超姚明”“想要上北大,没他可不行”等。
3.3.9医疗器械信息应当宣传和引导合理使用医疗器械,不得直接或间接怂恿公众购买使用,不得含有以下内容:
3.3.9.1含有不科学的表述或者通过渲染、夸大某种健康状况或者疾病所导致的危害,引起公众对所处健康状况或所患疾病产生担忧和恐惧,或使公众误解不使用该产品会患某种疾病或加重病情的;
3.3.9.2含有“家庭必备”或者类似内容的;
3.3.9.3含有评比、排序、推荐、指定、选用、获奖等综合性评价内容的;
3.3.9.4含有表述该产品处于“热销”、“抢购”、“试用”等的内容。
4 FAQ
4.1 问:客户仅做出口,认可的国外认证证书有哪些?
4.2 问:贸易公司没有《医疗器械注册证》或者国外认证证书,是提供工厂的吗?
答:是的
5 为什么制定这个规则?
为了保证医疗器械的安全、有效,保障人体健康和生命安全,遵守国家相关法律法规,只有取得相应资质的客户才能在中国制造网发布此类产品。
6 可参考的法律法规
7 违反规定会有怎么样的处罚措施?
不遵守我网发布规则,可能会导致一系列的操作,比如诚信分扣分、违规信息直接删除、相关类目限制发布、公司帐号暂停推广、永久关闭帐号不再合作等等。
8 附则
8.1
供应商的违规行为,发生在本管理规范生效之日以前的,适用当时的规范。发生在本管理规范生效之日以后的,适用本规范。
8.2
中国制造网可根据平台运营情况随时调整本管理规范并向客户公示。
8.3
供应商应遵守国家法律、行政法规、部门规章等规范性文件。对任何涉嫌违反国家法律、行政法规、部门规章等规范性文件的行为,本规范已有规定的,适用于本规范,本规范尚无规定的,依照法律法规处理。供应商依据相关规则承担的相关责任并不免除其应承担的法律责任。供应商在中国制造网的任何行为,应同时遵守与中国制造网及其关联公司签订的各项协议。
分享至: